Molalitas (kemolalan) menyatakan jumlah mol zat terlarut dalam 1 kg (1000g) pelarut.
m= (n x 1000) : p
*n = gr/mr (jumlah mol suatu zat)
*p= berat pelarut (gr)
molalitas untuk 2 zat atau campuran
m = [(m1 . p1)+ (m2+p2)] : (p1+p2)
Fraksi Mol menyatakan perbandingan antara jumlah mol salah satu komponen larutan dengan jumlah mol total larutan
Xa = na : (na+ nb)*Xa + Xb = 1
*Xa = fraksi mol
Contoh Soal Molalitas dan Fraksi Mol
1. Dicampurkan 975 gram larutan urea 5m dengan 340 gram larutan glukosa 3m. Kedua zat tidak saling bereaksi. Tentukan molalitas dan fraksi mol urea dan glukosa setelah dicampurkan!
urea = 5m, 975 gr --> 5 mol dalam 1000 gr pelarut
glukosa = 3m, 340 gr --> 3 mol dalam 1000 gr pelarut
gr urea (asumsi) = 5 x 60 = 300 gr
gr larutan = 1000 + 300 = 1300 gr
gr urea (sebenarnya) = 975/1300 x 300 = 225 gr
gr pelarut = 975 - 225 = 750 gr
gr glukosa (asumsi) = 3x180 = 540 gr
gr larutan = 1000 + 540 = 1540 gr
gr glukosa (sebenarnya) = 340/1540 x 540 = 119.22 gr
gr pelarut = 340 - 119.22 = 220,78 gr
m = [(m1 . p1)+ (m2+p2)] : (p1+p2)
= [(5x750)+(3x220,78)] : (750+220.78)
= 4.55 m
Xurea = nurea : (nurea + nglukosa + nair)
= (225/60): [(225/60) +(119.22/180) + (970.78 / 18)]
= 0.06
Xglukosa = nglukosa : (nurea + nglukosa + nair)
= (119.22/180) : [(225/60) +(119.22/180) + (970.78 / 18)]
= 0.01
SIFAT KOLIGATIF LARUTAN
Sifat suatu zat yang tidak bergantung pada jenis larutan, tetapi dipengaruhi oleh banyaknya partikel zat terlarut (konsentrasinya)
Sifat Koligatif Untuk Zat Non-elektrolit
1. Penurunan Tekanan Uap
Menguap adalah gejala yang terjadi saat molekul zat cair meninggalkan permukaan cairan dalam fase gas. Tekanan uap jenuh adalah tekanan maksimum uap pada suhu tertentu. Semakin mudah zat cair untuk menguap, semakin tinggi tekanan uapnya.
P = po . Xp
*Xp = fraksi mol zat pelarut
* P = tekanan uap jenuh larutan
* po = tekanan uap jenuh pelarut
*∆P = penurunan tekanan uap jenuh
* Xt = fraksi mol zat terlarut
"Tekanan uap jenuh pelarut lebih tinggi daripada tekanan uap jenuh larutan karena zat-zat terlarut menghalangi zat pelarut murni untuk menguap"
2. Kenaikan Titik Didih
Mendidih adalah proses penguapan di seluruh bagian zat cair dan terjadi pada titik didihnya. Jika suatu pelarut ditambahkan zat terlarut, maka titik didih larutan tersebut akan bertambah (karena tekanan uap jenuh larutan menurun).
∆Tb = m . Kb
*∆Tb = kenaikan titik didih
* Kb = tetapan titik didih molal (Ocm-1 )
3. Penurunan Titik Beku
Titik beku larutan selalu lebih rendah daripada titik beku pelarut karena zat terlarut menghambat pelarut untuk mengkristal.
∆Tf = m . Kf
*∆Tf = kenaikan titik beku
* Kf = tetapan titik beku molal (Ocm-1 )
4. Tekanan Osmotik
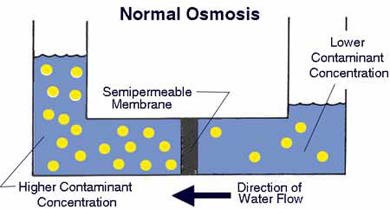
Osmosis adalah peristiwa terjadinya perpindahan molekul pelarut melalui pori-pori semipermeabel membran dari larutan yang lebih encer ke larutan yang lebih pekat (berkonsentrasi lebih tinggi). Berdasarkan Van Hoff, besarnya tekanan osmotik sama dengan tekanan gas menurut persamaan gas ideal.
P.V = n. R. T à P = n/V .R. T à π = M.R.T
* π = tekanan osmotik (atm)
*Tekanan Osmotik Pada Darah

Sifat Koligatif Untuk Zat Non-elektrolit
Elektrolit dibagi menjadi 3:
- biner ( cth: HCl, NaCl)
- tersier (cth: H2SO4, MgCl2)
- kuartener (cth: Al(OH)3, Fe(OH)3,H3PO4)
*Faktor Van't Hoff (i)
i = efek koligatif larutan elektrolit : efek koligatif larutan non elektrolit
i = efek koligatif larutan elektrolit : efek koligatif larutan non elektrolit
HCl --> 1 H+ + 1Cl-, n= 2 e kuat :
H2SO4 --> 2H+ + SO42-, n=3 e lemah : 0<
Elektrolit --> n. ion2 non elek :
i= 1 + (n-1)
*n = jumlah ion
*i = faktor Van't Hoff
*α = tetapan disosiasi
*n = jumlah ion
*i = faktor Van't Hoff
*α = tetapan disosiasi
Sifat
Koligatif
|
Non
elektrolit
|
Elektrolit
|
Tekanan
Osmotik
|
π = M.R.T
|
π = M.R.T. i
|
Kenaikan
Titik Didih
|
∆Tb
= m . Kb
|
∆Tb
= m . Kb.i
|
Penurunan
Titik Beku
|
∆Tf
= m. Kf
|
∆Tf
= m. Kf.i
|
Penurunan
Tekanan Uap
|
∆P
= po . Xt
|
∆P
= ( po . nt. i) : (nt.i + np)
|

Sumber:
- Chang, Raymond. 2006. Kimia Dasar: Konsep-Konsep Inti Jilid 2. Jakarta: Penerbit Erlangga
- Setiabudi, Agus, Yayan Sunarya. 2007. Mudah dan Aktif Belajar Kimia Untuk Kelas XII. Jakarta: PT Setia Purna Inves
- Sutresna, Nana. 2007. Kimia Untuk Kelas XII Semester 1. Bandung: Grafindo Media
- Huda, Mahfuzh. 2014. Pengertian dan Penerapan Sifat Koligatif Larutan. http://www.mystupidtheory.com/2014/07/pengertian-dan-penerapan-sifat.html diakses pada tanggal 29 November 2015
Sudah disusun dengan sistematis! Sangat membantu!
ReplyDeleteSangat bagus dan informatif! Nice!!!
ReplyDeleteBagus. Menarik dan informatif
ReplyDeleteWaahh komplit yah thankyou udh bantu buat belajar UAS ;)
ReplyDeletebagus sekali! saya jadi lebih mengerti terimakasih
ReplyDeletedetaill banget informatif! rapih dan bagus! sangat membantuu, makasih :)
ReplyDeleterapih banget, lengkap sama contohnya, informasi yang dikasih jelas dan lengkap. bagus banget!
ReplyDeleteBagus, unik, tampilan menarik
ReplyDeleteInformasinya lengkap, dapat membantu saya belajar karena informatif. Thankyouu😁
ReplyDeleteBlog ini cukup informatif dan lengkap dengan rumus rumus nya serta sumber yang valid. Nice blog! (:
ReplyDeletesaya merasa terbantu thankyou
ReplyDeleteinformasinya mudah dimengerti dan disertai gambar yang menarik!
ReplyDeleteInformasinya sangat membantu terima kasih :D
ReplyDeleteThankyou friend 😄
ReplyDelete